青书学堂河南科技大学物理化学(专升本)网上考试答案
| 简单低共熔混合物二组分系统液-固平衡中,低共熔点的自由度f=? |
| A:1 B:2 C:3 D:0 |
|
| 克拉普龙-克劳修斯方程的适用条件为? |
| A:单组分两相平衡,气相体积》液相体积 B:气体近似为理想气体,相变热不随温度而变 C:单组分两相平衡,气相体积《液相体积,气体近似为理想气体,相变热不随温度而变 D:单组分两相平衡,气相体积》液相体积,气体近似为理想气体,相变热不随温度而变 |
|
 |
| A:f = C - F +3 B:f = C+ F +3 C:f = C - F-3 D:f = C - F |
|
 度为? 度为? |
| A:0 B:1 C:2 D:3 |
|
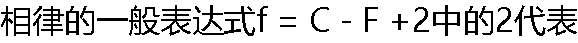 ? ? |
| A:2代表影响相平衡的外界条件为T和p两个因素 B:2代表影响相平衡的外界条件为T因素 C:2代表影响相平衡的外界条件为p因素 D:2代表影响相平衡的外界条件为T和e两个因素 |
|
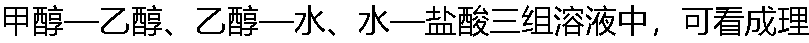 想溶液的是? 想溶液的是? |
| A:乙醇―水 B:甲醇―乙醇 C:水―盐酸 |
|
 ibbs函数,二种组分的物质的量分别是n1和n2,则体系的Gibbs函数G为? ibbs函数,二种组分的物质的量分别是n1和n2,则体系的Gibbs函数G为? |
| A:G = n1G1 + n2G2 B:G = n2G1 + n2G2 C:G= n2G1 - n2G2 D:G = n2G1 + n2G2 |
|
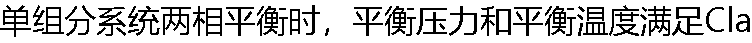 peyron方程? peyron方程? |
A: B: B: C: C: D: D: |
|
 式称为吸附? 式称为吸附? |
| A:等温式 B:不等温式 C:恒温式 D:变温式 |
|
 的平衡蒸气压的大小为p凸__p平___ P凹。 的平衡蒸气压的大小为p凸__p平___ P凹。 |
| A:> 、> B:< 、< C:> 、< D:=、> |
|
 晶析出的现象称为? 晶析出的现象称为? |
| A:过饱和现象 B:饱和现象 C:未饱和现象 |
|
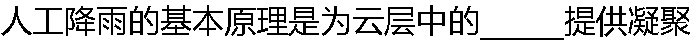 中心(如AgI颗粒)而使之成雨滴落下。 中心(如AgI颗粒)而使之成雨滴落下。 |
| A:过饱和水气 B:水气 C:云层 D:云层和水气 |
|
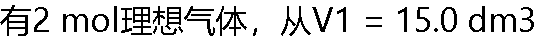 到V2 = 40.0 dm3,在298 K时,保持外压为100 kPa,做恒外压膨胀所做的功。 到V2 = 40.0 dm3,在298 K时,保持外压为100 kPa,做恒外压膨胀所做的功。 |
| A:-2.50 kJ B:2.50kj C:-3kj D:3kj |
|
| 有四种浓度均为 0.01 mol・kg -1 的电解质溶液,其中平均活度因子最大的是 |
| A:KCl B:CaCl2 C:Na2SO4 D:AlCl3 |
|
| 基元反应的分子数是个微观的概念,其值 |
| A:可为0、l、2、3 B:只能是1、2、3这三个正整数 C:也可是小于1的数值 D:可正,可负,可为零 |
|
| * 在一般情况下,电位梯度只影响 ( ) |
| A:离子的电迁移率 B:离子的迁移速率 C:电导率 D:离子承担的电流分数 |
|
| 下列有关反应级数的说法中,正确的是 |
| A:反应级数只能是大于零的数 B: 具有简单级数的反应都是基元反应 C:反应级数等于反应分子数 D:反应级数不一定是正整数 |
|
| * 稀溶液的依数性包括蒸 气 压下降、沸点升高、凝固点降低和渗透压,下面的陈述都与它们有关 , 其中正确的是 ( ) |
| A:只有溶质不挥发的稀溶液才有这些依数性 B:所有依数性都与溶液中溶质的浓度成正比 C:所有依数性都与溶剂的性质无关 D:所有依数性都与溶质的性质有关 |
|
| 下列说法中不正确的是 |
| A:平面液体没有附加压力 B:凸液面曲率半径为正,凹液面曲率半径为负 C:弯曲液面表面张力的方向指向曲率中心 D:弯曲液面的附加压力方向指向曲率中心 |
|
| 哪一种相变过程可以利用来提纯化学药品? |
| A:凝固 B:沸腾 C:升华 D:其中任一种 |
|
| 一个电池反应确定的电池, E 值的正或负可用来说明 |
| A:电池是否可逆 B:电池反应自发进行的方向和限度 C:电池反应自发进行的方向 D:电池反应是否达到平衡 |
|
| 化学反应的反应级数是个宏观的概念、实验的结果,其值 |
| A:只能是正整数 B:一定是大于1的正整数 C:可以是任意值 D: 一定是小于1的负数 |
|
| 天空中的水滴大小不等,在运动中,这些水滴的变化趋势如何? |
| A:大水滴分散成小水滴,半径趋于相等 B:大水滴变大,小水滴缩小 C:大小水滴的变化没有规律 D:不会产生变化 |
|
| * 下面的叙述中违背平衡移动原理的是 ( ) |
| A:升高温度平衡向吸热方向移动 B:增加压力平衡向体积缩小的方向移动 C:加入惰性气体平衡向总压力减少的方向移动 D:降低压力平衡向增加分子数的方向移动 |
|
若恒温不做非体积功情况下,3mol 理想气体自273K吸热Q1,若2mol该气体同样自273K升温到283K,吸热Q2,则有( ) |
| A:Q1 > Q2
B:Q1 < Q2 C:Q1 = Q2 D:无法比较Q1和Q2大小
|
|
| * 水不能润湿荷叶表面,接触角大于90°,当水中加入皂素后,接触角将 ( ) |
| A:变大 B:变小 C:不变 D:无法判断 |
|
| 使电解质溶液的平衡性偏离理想溶液的主要原因是 |
| A:电解质溶液能够导电 B: 电解质在溶液中只能部分电离 C:电解质溶液中的离子间存在静电引力 D:电解质溶液中的离子间存在分子引力 |
|
对于反应 ,如果反应物 A 的初始浓度减少一半, A 的半衰期增大 1 倍,则该反应为 ,如果反应物 A 的初始浓度减少一半, A 的半衰期增大 1 倍,则该反应为 |
| A:零级反应 B:一级反应 C:二级反应 D:三级反应 |
|
| 已知某反应的级数是一级,则可确定该反应一定 |
| A:简单反应 B:单分子反应 C:复杂反应 D:上述都不对 |
|
| 某反应无论反应物的起始浓度如何,完成 65% 反应的时间都相同,则反应的级数为 |
| A: 零级反应 B:一级反应 C: 二级反应 D:三级反应 |
|
| ?对于化学平衡,?以下说法中不正确的是 |
| A:化学平衡态就是化学反应的限度 B:化学平衡时系统的热力学性质不随时间变化 C:化学平衡时各物质的化学势相等 D:化学平衡跟温度没有关系 |
|
| ?下面的叙述中?不?违背平衡移动原理的是 |
| A:升高温度平衡向吸热方向移动 B:增加压力平衡向体积缩小的方向移动 C:加入惰性气体平衡向总压力减少的方向移动 D: 降低压力平衡向增加分子数的方向移动 |
|
| ?当克拉佩龙方程用于纯物质两相平衡时,下列说法不正确的是 |
| A:p一定不随温度而变化 B:?p?一定随温度的升高而降低 C:?p?一定随温度的升高而升高 D:?p?随温度的升高可能降低也可能升高 |
|
 O 4 与CO、CO 2 达到平衡时,其独立化学平衡数 R , 组分数 C 和自由度数 F 的叙述不正确的有 O 4 与CO、CO 2 达到平衡时,其独立化学平衡数 R , 组分数 C 和自由度数 F 的叙述不正确的有 |
| A:R = 3, C = 2, F = 0 B:R = 4, C = 1, F = 1 C:R = 1, C = 4, F = 2 D:R = 2, C = 3, F = 1 |
|
 制,其中 只能用 克拉佩龙方程 而不适合用 克-克方程 的 过程 有 制,其中 只能用 克拉佩龙方程 而不适合用 克-克方程 的 过程 有 |
| A:?I2(s)→I2(g) B:?C(石墨)→C(金刚石) C:?Hg2Cl2(s)→2HgCl(g) D:?N2(g,?T1,?p1)→N2(g,?T2,?p2) |
|
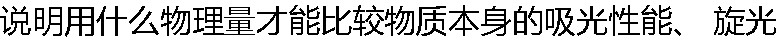 性能、折光性能和导电性能(指电解质)的大小,并说明每一物理量的物理意义。 性能、折光性能和导电性能(指电解质)的大小,并说明每一物理量的物理意义。 |
|
|

