����ѧ��¤��ѧԺ���˸ߵ�ѧ������ѧϰƽ̨������ѧʵ��(ר����)���Ͽ��Դ�
�ڵ��µ�ѹ�£�����Ӧ�� = 5kJ��mol ��1 ʱ���÷�Ӧ�ܷ����? �� �� = 5kJ��mol ��1 ʱ���÷�Ӧ�ܷ����? �� �� |
| A:�������Է����� B:�������Է����� C:�����ж� D:���ܽ��� |
|
  |
A: B: B: C: C: D: D: |
|
 |
A: B: B: C: C: D: D: |
|
 |
A: B: B: C: C: D: D: |
|
 |
A: B: B: C: C: D: D: |
|
*�ʵĶ���ʽ��  �� ʽ�е�P���� �� �� �� ʽ�е�P���� �� �� |
| A:��ϵ����ѹ�� B:��ϵ�и���ֵķ�ѹ C:100kPa D:��ѹ |
|
 |
A: B: B: C: C: D: D: |
|
 |
A: B: B: C: C: D: D: |
|
���������Һ̬������������ѹ�� �� |
| A:����Һ������� B:����������ֵ�����ѹ֮�� C:������һ����ֵ�����ѹ D:С����һ����ֵ�����ѹ |
|
 |
A: B: B: C: C: D: D: |
|
.373.15K��py�£�ˮ��Ħ��������Ϊ40.7kJ��mol-1��1molˮ�����Ϊ470px3��1molˮ���������Ϊ30 5000px3��1molˮ����Ϊˮ������DUΪ�� ���� |
| A:45.2kJ��mol-1 B:40.7kJ��mol-1 C:37.6kJ��mol-1 D:52.5kJ��mol-1 |
|
  |
A: B: B: C: C: D: D: |
|
 |
A: B: B: C: C: D: D: |
|
. Һ������T,p�����-�˷��̵������½��������Ĺ���,���¸��������в�����ǣ�( ) |
| A:Ħ������ѧ�� B:Ħ����� C:Ħ������˹���� D:Ħ���� |
|
.���з�Ӧ CaCO3(s) = CaO(s)+CO2(g) ��һ���¶��´�ƽ�⣬���ڲ��ı��¶Ⱥ�CO2 �ķ�ѹ����Ҳ���ı�CaO(s)�Ŀ�����С��ֻ����CaCO3(s)�Ŀ���ֱ�������ӷ�ɢ�ȣ���ƽ�⽫�� ���� |
| A:�����ƶ� B:�����ƶ� C:�������ƶ� |
|
. A(l)��B(l)���γ�����Һ̬��������һ���¶��£���A����B�ı�������ѹp*A��p*B�����ڸö���ֵ�����ѹ���ͼ�ϵ�����Һ����ƽ��������ƽ�������Һ�������ɱ���:( ) |
| A:y����x�� B:y����x�� C:y����x�� |
|
����һ��ѹ���£�������A�ķе㡢����ѹ�ͻ�ѧ�Ʒֱ�ΪTb*�� pA*��mA*�������������ӷ��Ե������γ���Һ֮��ֱ���Tb�� pA��mA������У� �� |
| A:Tb*<Tb�� pA*<pA�� ,mA*<mA B:Tb*>Tb�� pA*>pA�� ,mA*>mA C: Tb*>Tb�� pA*<pA�� ,mA*>mA D:Tb*<Tb�� pA*>pA�� ,mA*>mA |
|
1mol��ԭ���������壬��300Kʱ����ѹ����500K�������ʱ���HԼΪ(����) |
| A:4157J B:596J C:1255J D:994J |
|
. ��֪������е�б��б����Һ̬�����̬�����ִ���״̬�����������״̬____�ȶ����档 |
| A:�ܹ� B:���ܹ� C:��һ�� |
|
| Һ̬ˮ�� 100 �漰 101 . 325 kPa ��������ˮ��������ù��̵� |
| A:��H=0 B:��S=0 C:��A=0 D:��G=0 |
|
 |
| A:������ȷ����� B:ƽ��ʱ������ɺ�Һ�������ͬ�� C:��е�����ѹ�ı仯���仯 D:�뻯����һ������ȷ����� |
|
 |
A: B: B: C: C: D: D: |
|
 |
A: B: B: C: C: D: D: |
|
��25��ʱ��CH4(g)��H2O(l)��C6H6(l)�еĺ���ϵ���ֱ�Ϊ4.18��109Pa��57��106Pa ��������ͬ��ƽ�������ѹp(CH4)�£�CH4��ˮ�����ڱ��е�ƽ����ɣ� �� |
| A:x(CH4��ˮ) >x(CH4����) B:x(CH4��ˮ) <x(CH4����) C:x(CH4��ˮ) = x(CH4����) |
|
��40��ʱ����Һ��A�ı�������ѹ�Ǵ�Һ��B�����������A��B�ܹ�������Һ̬������ƽ�����������A��B��Ħ��������ȣ���ƽ��Һ�������A��B��Ħ������֮��xA:xB=( ) |
| A:1:2 B:2:1 C:3:2 D:4:3 |
|
. ����ı�Ħ��ȼ����Ϊ-3 520kJ��mol-1��CO2(g)��H2O(l)�ı�Ħ�������ʷֱ�Ϊ-395kJ��mol-1��-286kJ��mol-1��������ı�Ħ��������Ϊ�� �� |
| A:2 839kJ��mol-1 B:-2 839kJ��mol-1 C:171kJ��mol-1 D:-171kJ��mol-1 |
|
  |
A: B: B: C: C: D: D: |
|
 |
A: B: B: C: C: D: D: |
|
 |
A: B: B: C: C: D: D: |
|
. ϡ��Һ�����̵�Tf�봿�ܼ�Tf*�����̵�Ƚϣ�Tf lt;Tf*�������ǣ� �� |
| A:���ʱ����ǻӷ��Ե� B:�����Ĺ���һ���ǹ����� C:�����Ĺ����Ǵ��ܼ� D:�����Ĺ����Ǵ����� |
|
 |
A: B: B: C: C: D: D: |
|
���»�����ʽ��Ϊʵ��������Ϊ�������崦��ʱ��Ӧ�����У��������ĿΪ(����) |
| A:4 B:3 C:2 D:1 |
|
. A��B������ڶ��¶�ѹ�»���γ�����Һ̬�����ʱ�����У��� ���� |
| A:DmixH=0 B:DmixS=0 C:DmixA=0 D:DmixG=0 |
|
�ڻ��������ѹ����λ�У���1atm�൱����Щ������ϵ���Dz��Ե�(����) |
| A:101325Pa B:1.01325bar C:76torr D:760mmHg |
|
 |
A: B: B: C: C: D: D: |
|
. ���A��B�γ�����Һ̬���� ��֪��100��ʱ�����A������ѹΪ133.32kPa�������B������ѹΪ66.66kPa����A��B�������Һ̬����������A��Ħ������Ϊ0.5ʱ����Һ̬������ƽ��������У����A��Ħ�������ǣ� �� |
| A:1 B:? C:2/3 D:1/2 |
|
. ��a��b�����ж�����A��B�������ʣ����ﵽ��ƽ��ʱ���������������ȷ���ǣ� �� |
A: B: B: C: C: |
|
*�ʵĶ���ʽ��  �� ʽ�е�P���� �� �� �� ʽ�е�P���� �� �� |
| A:��ϵ����ѹ�� B:��ϵ�и���ֵķ�ѹ C:100kPa D:��ѹ |
|
 |
A: B: B: C: C: D: D: |
|
��ָ�����ں������ɵ����м���˵���У�������ǣ� �� |
| A:��������������ܼ��еķ���״̬������ͬ B:���ʱ����Ƿǻӷ��Ե� C:�¶�����ѹ�����ͣ���Һ��ϡ������������ȷ D:���ڻ�����壬����ѹ����̫��ʱ�����������ֱܷ�������ÿһ�����壬����������ķ�ѹ�� |
|
| ���ڻ�ѧƽ��, ����˵���в���ȷ���� |
| A:��ѧƽ��̬���ǻ�ѧ��Ӧ���� B:��ѧƽ��ʱϵͳ������ѧ���ʲ���ʱ��仯 C:��ѧƽ��ʱ�����ʵĻ�ѧ����� D:��ѧƽ�����¶�û�й�ϵ |
|
 �ǣ� �ǣ� |
| A:���� B:��ѹ C:����������� D:���ϵͳ |
|
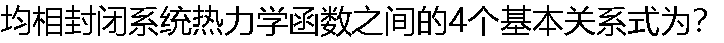 |
| A:dU = TdS �C pdV B:dH = TdS + Vdp C:dA = �C SdT �C pdV D:dG = �C SdT + Vdp |
|
| �����ϵͳ��ͼ���Ը��ݿ�-�˷��̺Ϳ����������������ƣ����� ֻ���� ������������ �����ʺ��� ��-�˷��� �� ���� �� |
| A:I2(s)��I2(g) B:C(ʯī)��C(���ʯ) C:Hg2Cl2(s)��2HgCl(g) D:N2(g, T1, p1)��N2(g, T2, p2) |
|
| ����Fe��FeO��Fe 3 O 4 ��CO��CO 2 �ﵽƽ��ʱ���������ѧƽ���� R , ����� C �����ɶ��� F ����������ȷ���� |
| A:R = 3, C = 2, F = 0 B:R = 4, C = 1, F = 1 C:R = 1, C = 4, F = 2 D:R = 2, C = 3, F = 1 |
|
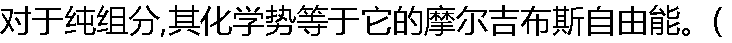 ) ) |
| A:��ȷ B:���� |
|
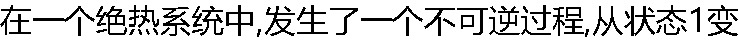 ��״̬2,������ʲô����,ϵͳ��Ҳ�ز���ԭ��״̬�ˡ�( ) ��״̬2,������ʲô����,ϵͳ��Ҳ�ز���ԭ��״̬�ˡ�( ) |
| A:��ȷ B:���� |
|
 ��ƽ����ɡ�( ) ��ƽ����ɡ�( ) |
| A:��ȷ B:���� |
|
 ���ͬʱ�õ���������֡�( ) ���ͬʱ�õ���������֡�( ) |
| A:��ȷ B:���� |
|
 |
| A:��ȷ B:���� |
|
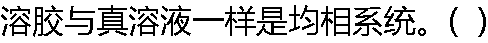 |
| A:��ȷ B:���� |
|
 |
| A:��ȷ B:���� |
|
 �ݣ������ǿ�����̡� �ݣ������ǿ�����̡� |
| A:��ȷ B:���� |
|
��ߵ�����Դ���¶ȷֱ���T1��T2����Carnot�Ȼ���Ч�ʦ�Ϊ  �� �� |
| A:��ȷ B:���� |
|
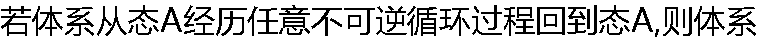 ���ر���ܴ�����,Ҳ����С���㡣( ) ���ر���ܴ�����,Ҳ����С���㡣( ) |
| A:��ȷ B:���� |
|
���ϵͳ����ѧ��һ���ɵ���ѧ����ʽΪ  �� �� |
| A:��ȷ B:���� |
|
����ѧ�ڶ����ɵ���ѧ����ʽ(Clausius����ʽ)����ʽ��  �� �� |
| A:��ȷ B:���� |
|
 ��( ) ��( ) |
| A:��ȷ B:���� |
|
 ) ) |
| A:��ȷ B:���� |
|
| ���Ǧ�G gt;0�Ĺ��̶����ܽ��С�( ) |
| A:��ȷ B:���� |
|

