����ѧ�ú���������ѧ��ѧ��ѧ(ר����)���Ͽ��Դ�
 |
| A:�����˷�Ӧ�Ļ�� B:����Ӧ��֮�����ײƵ�� C:��С�����ʳ���ֵ D:������ƽ�ⳣ��ֵ |
|
| �¶�ΪTʱ, ����㶨ΪV����������A��B����ֵĻ����������, ��ѹ���ֱ�ΪpA��pB.����������ע��n Ħ������������C, ��A��B�ķ�ѹ:( ) |
| A:������ B:pA����,pB��С C:pA��С,pB���� D:������ |
|
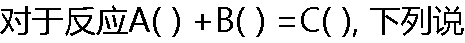 ����,��ȷ����( ) ����,��ȷ����( ) |
| A:��Ӧ�������ڷ�Ӧ������; B:��Ӧ����С�ڷ�Ӧ������; C:��Ӧ�������ڷ�Ӧ������; D:����ȷ����Ӧ�����ͷ�Ӧ�������ĸ��� |
|
��Ag�缫��AgNO3��Һ�������뺬Zn�缫��Zn(NO3)2��Һ����, ��һ��ر���ʽ��ȷ����( )
��֪[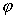 ��(Zn2+/Zn)=-0.76V, ��(Zn2+/Zn)=-0.76V, 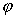 ��(Ag+/Ag)=0.80V] ��(Ag+/Ag)=0.80V] |
| A:(-)Ag|Ag+(c1)��Zn2+(c2) |Zn (+) B:(-)Zn|Zn2+(c2)��Ag+(c1) |Ag (+) C:(-) Zn2+(c2) |Zn��Ag+(c1) |Ag (+) D:(-) Ag+(c1)| Ag��Zn2+(c2) |Zn (+) |
|
| �������������γ������������,ʹ�۽�������Mn2+,Co2+,Ni2+��Fe3+,Al3+���ӷ���,Ӧ������Һ��pHΪ( ) |
| A:5~6 B:6~7 C:7~8 D:8~10 |
|
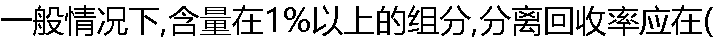 ) ) |
| A:90~95% B:95~99% C:99%���� D:100% |
|
 ϵ( ) ϵ( ) |
| A:������ B:������˹�ط��� C:������ɢ������ʽ D:��Ũ�ȵĶ����ɷ��� |
|
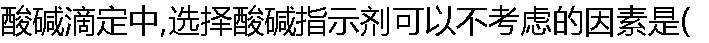 ) ) |
| A:pHͻԾ��Χ B:ָʾ���ı�ɫ��Χ C:ָʾ����Ħ������ D:Ҫ�����Χ |
|
 |
| A:������ B:û��Ҫ�� C:�Դ���������� D:��������Χ֮�� |
|
 |
| A: F B:C1 C:Na D:H |
|
 |
| A: n=3, l=1, m=-1 B:n=3,l=1, m=2 C:n=2,1=2, m=-1 D:n=4,1=-2,m=1 |
|
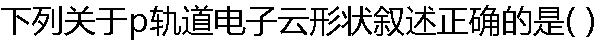 |
| A:���ζԳ� B:8����ƽ�� C:����ֵ��x.y.z���ϵ�˫���� D:���ഹֱ��÷������ |
|
һ��ѧ��Ӧϵͳ�ڵ��¶��������·���һ�仯,��ͨ��W����ͬ��;�����:
(1)����10 kJ,���繦50 kJ;;(2)����o,������,��( ) |
| A:Q=-60kJ B: Q=-10 kJ C: Q=-40kJ D:��Ӧ��Qv=-10kJ |
|
| �ܽ����о۽�ȶ���,�����������Fe(OH)3�ܽ����Դ����������۳�,��ԭ����( ) |
| A:����IJ����˶� B:����Ķ����ЧӦ C:�������ܼ���Ĥ D:��������ͽ������ܼ���Ĥ |
|
 |
| A:1,2 B:0,1,2 C:1,2,3 D:0,+1,-1 |
|
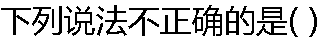 |
| A:��ԭ����,���ӵ�����ֻȡ������������n B:�����ԭ����,���ӵ�����������n�й�,����1�й� C:���������ĸ�������ȷ�� D:����Ѧ���̵ĺ�����,��Ϊ������ |
|
| Ҫ����Fe2+�ı���Һ,��õķ����ǽ�( ) |
| A:�������������ˮ B: FeC12����ˮ C:��������ϡ�� D: FeCl 2��Һ����м��Ӧ |
|
 |
| A:������ B:����� C:�ⲻ�� D:ά���ز��� |
|
��֪��(Sn4+/Sn2+)=0.15V,��(Cu2+/Cu)=0.34V,��(Fe3+/Fe2+)=0.77V,
��(Cl2/Cl-)=1.36V, �ڱ�״̬�����Է����еķ�Ӧ��( ) |
| A: Cl2+Sn2+ 2Cl-+Sn4+ B: 2Fe2++Cu2+ 2Fe3++Cu C:2Fe2++Sn4+ 2Fe3++Sn2+ D:2Fe2++Sn2+ 2Fe3++Sn4+ |
|
 ����������������( ) ����������������( ) |
| A: c(A2+)��c2(B-)>Ksp B: c(A2+)��c2(B-)< Ksp C: c(A2+)��c(B-)>Ksp D: c(A2+)��c(B-)< Ksp |
|
| ��֪CaCO3��Ks=4.96��10-9,��CaCO3(s)��c(CaCl2)=0.0010 mol��dm-3��CaCl2��Һ�е��ܽ��S��( ) |
| A:4.96��10-6 mol��dm-3 B:4.96��-8mol��dm-3 C:4.96��10-5 mol��dm-3 D:7.04��10-3 mol��dm-3 |
|
| ��298K,��ӦBaCl2��H2O(s)=BaCl2(s)+H2O(g)��ƽ��ʱ��p(H2O)=330Pa����Ӧ��K?Ϊ( ) |
| A: 3.3 B: 9.9 C: 100 D: 10.89 |
|
 )�� )�� |
| A: ɫɢ�� B: �յ��� C: ȡ���� D: ��� |
|
| ���ڷ�Ӧ Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O,�䦤rGm= �CnFE,ʽ��n����( )�� |
| A: 1 B: 6 C: 3 D: 12 |
|
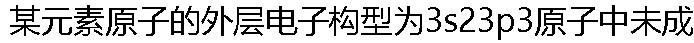 �Ե�����Ϊ( )�� �Ե�����Ϊ( )�� |
| A: 1 B: 2 C: 3 D: 0 |
|
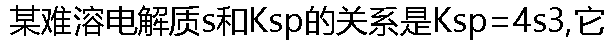 �ķ���ʽ������( )�� �ķ���ʽ������( )�� |
| A: AB B: A2B3 C: A3B2 D: A2B |
|
| ��֪�缫��ӦCu2++2e- = Cu�Ħզ�Ϊ0.34V,��缫��Ӧ:2Cu - 4e- = 2Cu2+��ֵΪ( ) |
| A: - 0.68V B: +0.68V C: - 0.34V D: 0.34V |
|
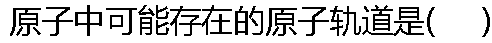 |
| A:n=1, l=2, m=0, ms=+ B:n=2, l=1, m=1, ms=- C:n=3, l=3, m=3, ms=- D:n=3, l=2, m=3, ms=+ |
|
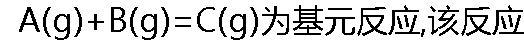 �ļ���Ϊ()�� �ļ���Ϊ()�� |
| A: 1 B: 2 C: 3 D: 0 |
|
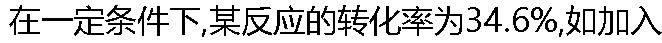 ����,�÷�Ӧ��ת���ʽ���( )�� ����,�÷�Ӧ��ת���ʽ���( )�� |
| A: ����34.6% B: С��34.6% C: ����34.6% D: ����ȷ�� |
|
 ����( )�� ����( )�� |
| A:�й�������ѧ�������ߡ������� B:�ɹ���������ȡ���ķ������������� C:�����Ƽ�Ĵ����ߡ�����°� D:�й����廯ѧ��ҵ֮���������� |
|
 |
| A:���ֵ��ЧӦ�͵�ⶨ�� B:�����ĺ���ѧ˵ C:��һ�����ֱ�,���о������� D:������ȫ��� |
|
 |
| A:�����ϴٽ��˻�ѧ���۵ķ�չ B:Ӧ���ϴٽ���ú���ͻ�ѧ��ҵ C:������ҵ��ú����ҵ�Ĺ��� D:ָ����Ⱦ�ϡ�ҩƷ��ըҩ���л���Ʒ�Ľ�һ���ϳ� |
|
 ȥ������ƿ����Һ���������ó�ƿ�⣬�궨����() ȥ������ƿ����Һ���������ó�ƿ�⣬�궨����() |
| A:ƫ�� B:ƫ�� C:��һ�� D:��Ӱ�� |
|
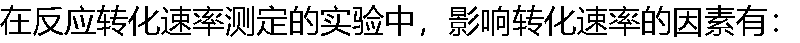 ���� ���� |
| A:��Ӧ��Ũ�� B:��Ӧʱ�� C:��Ӧ�¶� D:���� |
|
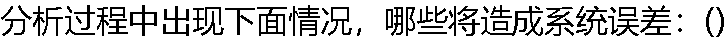 |
| A:��ƽ���ͻȻ�б䶯 B:�ֹ��ȼƵ�����в��� C:�ζ��ܶ������һλ���� D:�Ժ���Ϊ98%����ɰ�궨HClŨ�� |
|
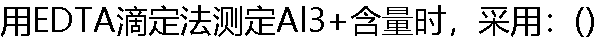 |
| A:���ζ��� B:PAN��ָʾ�� C:����T��ָʾ�� D:��ָʾ�� |
|
 ����ʲô?��һ��Ļ�ѧ��Ӧ,���ʷ���ʽ�ķ�Ӧ�����ܷ�ֱ�Ӹ��ݻ�ѧ��Ӧ����ʽ��д?Ϊʲô? ����ʲô?��һ��Ļ�ѧ��Ӧ,���ʷ���ʽ�ķ�Ӧ�����ܷ�ֱ�Ӹ��ݻ�ѧ��Ӧ����ʽ��д?Ϊʲô? |
|
|

