����ѧ�ú���������ѧ������ѧ(ר����)���Ͽ��Դ�
 |
A: ; B:EDTA; C:RSD; D:Ksp; E:Ka ; B:EDTA; C:RSD; D:Ksp; E:Ka |
|
 |
A: ; B:EDTA; C:RSD; D:Ksp; E:Ka ; B:EDTA; C:RSD; D:Ksp; E:Ka |
|
 |
A: ; B:EDTA; C:RSD; D:Ksp; E:Ka ; B:EDTA; C:RSD; D:Ksp; E:Ka |
|
 |
A: ; B:EDTA; C:RSD; D:Ksp; E:Ka ; B:EDTA; C:RSD; D:Ksp; E:Ka |
|
| �����ĸ����Ŵ�����Ա�ƫ��( ); |
A: ; B:EDTA; C:RSD; D:Ksp; E:Ka ; B:EDTA; C:RSD; D:Ksp; E:Ka |
|
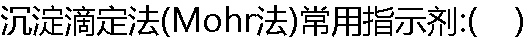 |
| A:�ᾧ��; B:��̪; C:����-KI; D:����T; E:����� |
|
 |
| A:�ᾧ��; B:��̪; C:����-KI; D:����T; E:����� |
|
 |
| A:�ᾧ��; B:��̪; C:����-KI; D:����T; E:����� |
|
 |
| A:�ᾧ��; B:��̪; C:����-KI; D:����T; E:����� |
|
 |
| A:�ᾧ��; B:��̪; C:����-KI; D:����T; E:����� |
|
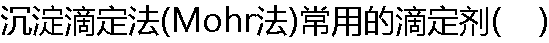 |
| A:HCl; B:EDTA ; C:I2; D:HClO4; E:AgCl |
|
 |
| A:HCl; B:EDTA ; C:I2; D:HClO4; E:AgCl |
|
 |
| A:HCl; B:EDTA ; C: I2 D:HClO4; E:AgCl |
|
 |
| A:HCl; B:EDTA ; C: I2 D:HClO4; E:AgCl |
|
 |
| A:HCl; B:EDTA ; C: I2 D:HClO4; E:AgCl |
|
 |
| A:3; B:4 ; C:5; D:6 |
|
 ) ) |
| A:�CC=S; B:�COH; C:�CN=N- ; D:�CCH3 |
|
 |
| A:��缫 B:���缫 C:�����缫 D:��-�Ȼ����缫 |
|
 |
| A:c��10-8(mol/L) B:c / Ka�� 500 C:c ? Ka �� 20K D:c ? Ka gt; 10-8 |
|
| ij���ָʾ����KHIn=1.0��10-5,�����۱�ɫ��Χ��pH( )�� |
| A:4-5 B:5-6 C:5-7 D:4-6 |
|
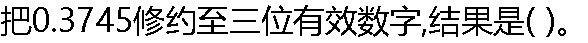 |
| A: 0.374 B: 0.375 C: 0.37 D: 0.370 |
|
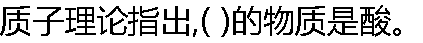 |
| A:�����H+ B:�����OH- C:�������� D:�������� |
|
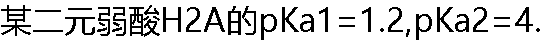 2����ʹHA-Ϊ��Ҫ������ʽ,���轫��ҺpH������( ) 2����ʹHA-Ϊ��Ҫ������ʽ,���轫��ҺpH������( ) |
| A: lt;1.2 B:1.2-4.2 C: gt;4.2 D: gt;5.2 |
|
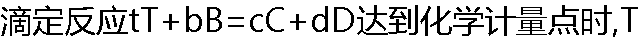 �����ʵ�����B�����ʵ����Ĺ�ϵ��( )�� �����ʵ�����B�����ʵ����Ĺ�ϵ��( )�� |
| A:1:1 B:t:b C:b:t D:��ȷ�� |
|
 |
| A: ���������ȷ�� B: ��������ľ��ܶȺ�ȷ�� C: ��������ľ��ܶ� D: ƽ��ֵ�ľ������ |
|
 |
| A:�ڲ��Ͻ����½��� B:�ڽ�Ũ��Һ�н��г��� C:������Һ�н��г��� D:����Ӧ����һ��ʱ����ٳ»� |
|
 |
| A:Ũ���䡢���������� B:ϡ���䡢���������� C:ϡ���ȡ����������� D: ϡ���ȡ��졢������ |
|
 |
| A:Ѹ�ٳ�ȡһ��������NaOH,�ܽ��������ƿ���� B:��ȡһ������NaOH,�ܽ��ϡ�͵�һ�����,�ٱ궨 C:�ڷ�����ƽ��ȷ��ȡһ������NaOH,�ܽ������Ͳ���� D:�ڷ�����ƽ��ȷ��ȡһ������NaOH,�ܽ��������ƿ���� |
|
 |
| A:c����,KaԽС��ΧԽ�� B: c����,KaԽ��ΧԽխ C:Ka����,cԽС��ΧԽխ D: Ka����,cԽС��ΧԽ�� |
|
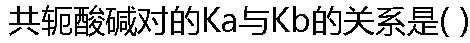 |
| A: Ka��Kb = 1 B:Ka��Kb = KW C: Ka/Kb=KW D:Kb/Ka=KW |
|
 ��( ) ��( ) |
| A:��Ӧ�ٶȿ�,ȱ����ɫ�����ָʾ�� B:��Ӧ��������ȫ,��Ӧ�ٶ��� C:���ɵ�����ﲻ�ȶ� D:���ϵζ�������Ҫ�����к��ʵ�ָʾ�� |
|
 |
| A:ָʾ�������۱�ɫ��(pKHIn) B:ָʾ���ı�ɫ��Χ C:ָʾ������ɫ�仯 D:�ζ�ͻԾ��Χ |
|
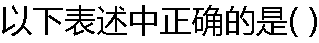 |
| A:H2O��Ϊ��Ĺ������OH- B:H2O��Ϊ��Ĺ�������H3O+ C:��ΪHAc������ǿ,��HAc�ļ��Ա��� D:HAc��Ϊ��Ĺ������Ac- |
|
 |
| A:��ȷ������ B:ȷ�ر궨 C:���б���Һ���뵱���䡢����ꡢ������ D:�궨����Һ��Ũ��ʱ,һ����ƽ�б궨����,������侫�ܶ� |
|
 |
| A:���ջ�ѧ��Ӧ�IJ�ͬ,�ζ��������ɷ�Ϊ����������λ��������ԭ�ȵζ��� B:ֻҪ�������Ի���Ե����ʶ��������ζ����ⶨ�京�� C:���ζ�����������ת�Ʒ�ӦΪ������һ�ֵζ������� D:ֻҪ�ǻ�ѧ��Ӧ�ܽ�����ȫ,�Ϳ�������ֱ�ӵζ� |
|
 |
| A:����Ӧ������Һ�н��� B:����Ӧ��Ũ����Һ�н��� C: ����Ӧ���ù�ҹʹ�����»� D:����ʱ�������ʻ�ijЩ��������������۵Ľ��� |
|
 |
| A:0.040 B:pH=4.22 C: 21 D:23.0% |
|
 ������������( ) ������������( ) |
| A:��ɫӦ��ָʾ��������ɫһ�� B:��ɫӦ��ָʾ��������ɫ���������� C:�ȶ���С�ڽ���-EDTA����� D:�ȶ��Դ��ڽ���-EDTA����� |
|
 |
| A:���� B:���� C: ��̪ D:�����̪(pKHIn=10.0) |
|
 |
| A:H20���ܽ����������ܸ�������,�������������� B: NH4+�Ĺ������NH3 C:��Ӧʵ�������ӵ�ת�Ʒ�Ӧ D:����������Ǵ���Ĺ����� |
|
��ȡ0.5000 gij��һԪ����HB����������ˮ��ϡ��50.00 mL����0.1000 mol/L NaOH��Һ�ζ����ӵ�λ�ζ����ߵõ���������: V (NaOH)/mL 0.00 20.47 40.94(��ѧ������) pH 2.65 4.21 8.43 �Լ����һԪ����HB��Ħ��������pKaֵ����ѧ������ǰ���0.1%ʱpH�� |
|
|

