青书学堂陇东学院成人高等学历教育学习平台物理化学(专升本)网上考试答案
| 涉及溶液表面吸附的说法中正确的是 |
| A:溶液表面发生吸附后表面自由能增加 B:溶液的表面张力一定小于溶剂的表面张力 C:定温下,表面张力不随浓度变化时,浓度增大,吸附量不变 D:饱和溶液的表面不会发生吸附现象 |
|
| * 某理想气体进行绝热自由膨胀,其热力学能和焓的变化为( ) |
A: B: B: C: C: D: D: |
|
| * 固体Fe、FeO、Fe 3 O 4 与CO、CO 2 达到平衡时,其独立化学平衡数 R , 组分数 C 和自由度数 F 分别为 ( ) |
| A:R = 3, C = 2, F = 0 B:R = 4, C = 1, F = 1 C:R = 1, C = 4, F = 2 D:R = 2, C = 3, F = 1 |
|
 ( )。 ( )。 |
| A:水 B:乙醇 C:环己烷 |
|
| 应用能斯特方程计算出电池 E < 0 ,这表示电池的反应是 |
| A:不可能进行 B:反向自发进行 C:正向自发进行 D:反应方向不确定 |
|
| * 0.001mol・kg -1 K 3 [Fe(CN) 6 ] 水溶液的离子强度为 ( ) |
| A:6.0×103 B:5.0×103 C:4.5×103 D:3.0×103 |
|
| 真实气体经历自由膨胀过程,系统的△U和温度变化△T有( ) |
| A:=0,=0 B:≠0,=0 C:=0,≠0 D:≠0,≠0 |
|
 |
| A:2H2(g) + O2(g)→ 2H2O(g) B:CO(g) +?O2(g)→ CO2 (g) C:H2(g) +?O2(g)→ H2O(l) D:4C(石墨)+3H2(g) → C2H2(g) +C2H4(g) |
|
| 298.15K、P?下液态水的化学势μ(l),水蒸汽的化学势μ(g),则( ) |
| A:μ(l) = μ(g) B:μ(l) < μ(g) C:μ(l) > μ(g) D:μ(l) ≠ μ(g) |
|
对于反应 ,如果反应物 A 的初始浓度减少一半, A 的半衰期增大 1 倍,则该反应为 ,如果反应物 A 的初始浓度减少一半, A 的半衰期增大 1 倍,则该反应为 |
| A:零级反应 B:一级反应 C:二级反应 D:三级反应 |
|
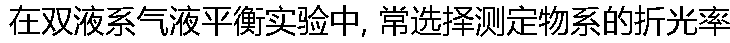 来测定物系的组成。下列哪种??选择的根据是不对的??( ) 来测定物系的组成。下列哪种??选择的根据是不对的??( ) |
| A: 测定折光率操作简单 B: 对任何双液系都能适用 C: 测定所需的试样量少 D: 测量所需时间少, 速度快 |
|
若恒温不做非体积功情况下,3mol 理想气体自273K吸热Q1,若2mol该气体同样自273K升温到283K,吸热Q2,则有( ) |
| A:Q1 > Q2
B:Q1 < Q2 C:Q1 = Q2 D:无法比较Q1和Q2大小
|
|
 |
| A: 标准物质法 B: `电位滴定法 C: 电加热法 D: 酸碱滴定法 |
|
 =0 的过程应满足的条件是 =0 的过程应满足的条件是 |
| A:等温等压且非体积功为零的可逆过程 B:等温等压且非体积功为零的过程 C:等温等容且非体积功为零的过程 D:可逆绝热过程 |
|
 ) ) |
| A:雷诺曲线 B:溶解度曲线 C:标准曲线 D:吸热――放热曲线 |
|
| * 非理想气体在绝热条件下,向真空膨胀后,下述答案中不正确的是( ) |
A:Q=0 B: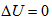 C:W=0 D: C:W=0 D: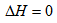 |
|
| 某反应进行时,反应物浓度与时间成线性关系,则此反应的半衰期与反应物初始浓度的关系是 |
| A:成正比 B:成反比 C:平方成反比 D:无关 |
|
* 在等温等压下,当反应的 = 5kJ・mol -1 时,该反应能否进行? ( ) = 5kJ・mol -1 时,该反应能否进行? ( ) |
| A:能正向自发进行 B:能逆向自发进行 C:不能判断 D:不能进行 |
|
| 在一定的 T,p 下,某真实气体的Vm,真实 大于理想气体的Vm,真实 ,则该气体的压缩因子Z( ) |
| A:大于1 B:小于1 C:等于1 D:无法判断 |
|
 ibbs函数,二种组分的物质的量分别是n1和n2,则体系的Gibbs函数G为? ibbs函数,二种组分的物质的量分别是n1和n2,则体系的Gibbs函数G为? |
| A:G = n1G1 + n2G2 B: G = n2G1 + n2G2 C: G= n2G1 - n2G2 D: G = n2G1 + n2G2 |
|
| 化学反应的反应级数是个宏观的概念、实验的结果,其值 |
| A:只能是正整数 B:一定是大于1的正整数 C:可以是任意值 D: 一定是小于1的负数 |
|
| 某理想气体进行绝热自由膨胀,其热力学能和焓的变化为( ) |
A: B: B: C: C: D: D: |
|
| 若已知某反应的△rCp,m=0,则当温度升高时该反应的△rSθm( ) |
| A:不能确定 B:增大 C:减小 D:不变 |
|
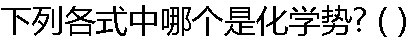 |
A: B: B: C: C: D: D: |
|
 的?( )。 的?( )。 |
| A:贝克曼温度计与水银接触温度计 B:贝克曼温度计和普通水银温度计 C:水银接触温度计和普通水银温度计 |
|
 浓度变化,可用物理法,选用的的测量仪器是( )。 浓度变化,可用物理法,选用的的测量仪器是( )。 |
| A:折光仪 B:电导仪 C:旋光仪 |
|
| 天空中的水滴大小不等,在运动中,这些水滴的变化趋势如何? |
| A:大水滴分散成小水滴,半径趋于相等 B:大水滴变大,小水滴缩小 C:大小水滴的变化没有规律 D:不会产生变化 |
|
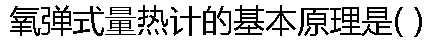 |
| A: 能量守恒定律 B: 质量作用定律 C: 基希基希霍夫定律 D: 以上定律都适用 |
|
| CaCO3(s) === CaO(s) + CO2(g)的标准平衡常数为Kθ,则CaCO3的分解压p=? |
A: B: K p C: B: K p C: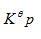 D: D: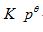 |
|
| 动力学研究中,任意给定的化学反应 A + B → 2D ,是 |
| A:表明为二级反应 B:表明是双分子反应 C:表示了反应的计量关系 D:表明为基元反应 |
|
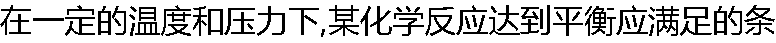 件是( ) 件是( ) |
| A:ΔG?=0 B:ΔG=0 C:ΔG=ΔG? D:ΔG?=-RTlnk? |
|
某理想气体的 ,则该气体应为 ,则该气体应为 |
| A:单原子分子气体 B:双原子分子气体 C:三原子分子气体 D:四原子分子气体 |
|
| 水中加入表面活性剂后将发生 |
A: ,正吸附 B: ,正吸附 B: ,负吸附 C: ,负吸附 C: ,正吸附 D: ,正吸附 D: ,负吸附 ,负吸附 |
|
 度为? 度为? |
| A:0 B: 1 C: 2 D: 3 |
|
| 某液体物质在恒温恒压条件下蒸发为蒸气,过程的△U( ) |
| A:大于0 B:等于0 C:小于0 D:无法确定 |
|
 |
| A:体积差ΔmixV =0,熵变ΔmixS > 0 B: 体积差ΔmixV<0,熵变ΔmixS= 0 C: 体积差ΔmixV =0,熵变ΔmixS< 0 D: 体积差ΔmixV >0,熵变ΔmixS > 0 |
|
 |
| A:通过相图可确定一定条件下体系由几相构成 B:相图可表示出平衡时每一相的组成如何 C:相图可表示出达到相平衡所需的时间长短 D:通过杠杆规则可在相图上计算各相的相对数量多少 |
|
| 1000K下,多组分多相平衡系统有C(石墨),CO(g),CO2(g)及O2(g)共存,物质间存在下化学平衡: C(石墨)+O2(g)→CO2(g) C(石墨)+O2(g)→CO(g) CO(g)+O2(g)→CO2(g) 则此平衡系统的组分数C, 相数P以及自由度数F分别是() |
| A:2,2,2 B:2,2,1 C:4,1,2 D:1,2,1 |
|
对于反应 ,如果反应物 A 的初始浓度减少一半, A 的半衰期增大 1 倍,则该反应为 ,如果反应物 A 的初始浓度减少一半, A 的半衰期增大 1 倍,则该反应为 |
| A:零级反应 B:一级反应 C:二级反应 D:三级反应 |
|
封闭系统热力学第一定律的数学表达式为  。 。 |
| A:正确 B:错误 |
|
| 293K时,0.50 kg 水(A)中溶有甘露糖醇(B)2.597 × 10-2 kg,该溶液的蒸气压为2322.4 Pa。已知这该温度时,纯水的蒸气压为2334.5Pa。甘露糖醇的摩尔质量MB=0.181 kg ? mol-1,正确吗? |
| A:正确 B:错误 |
|
设高低温热源的温度分别是T1和T2,则Carnot热机的效率η为  。 。 |
| A:正确 B:错误 |
|
 馏可同时得到两个纯组分。( ) 馏可同时得到两个纯组分。( ) |
| A:正确 B:错误 |
|
 饱和蒸气压之间,这种说法正确。 饱和蒸气压之间,这种说法正确。 |
| A:正确 B:错误 |
|
| 凡是ΔG gt;0的过程都不能进行。( ) |
| A:正确 B:错误 |
|
封闭系统热力学第一定律的数学表达式为  。 。 |
| A:正确 B:错误 |
|
热力学第二定律的数学表达式(Clausius不等式)的微分式是  。 。 |
| A:正确 B:错误 |
|
 到状态2,不论用什么方法,系统再也回不到原来状态了。( ) 到状态2,不论用什么方法,系统再也回不到原来状态了。( ) |
| A:正确 B:错误 |
|
设高低温热源的温度分别是T1和T2,则Carnot热机的效率η为  。 。 |
| A:正确 B:错误 |
|
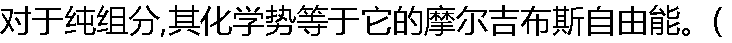 ) ) |
| A:正确 B:错误 |
|
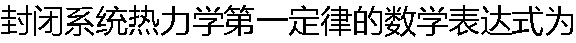 |
| A:正确 B:错误 |
|
 据,过程是可逆过程。 据,过程是可逆过程。 |
| A:正确 B:错误 |
|
封闭系统热力学第一定律的数学表达式为  。 。 |
| A:正确 B:错误 |
|
 过程。 过程。 |
| A:正确 B:错误 |
|
 )的微分式是 )的微分式是 |
| A:正确 B:错误 |
|
封闭系统热力学第一定律的数学表达式为  。 。 |
| A:正确 B:错误 |
|
 ) ) |
| A:正确 B:错误 |
|
 分别都处于各自所选定的标准态,是错误的。 分别都处于各自所选定的标准态,是错误的。 |
| A:正确 B:错误 |
|

